舒沃替尼针对20号外显子非小细胞肺癌单药最佳肿瘤缓解率高达48.4%,肺癌领域的巨大潜力再获国际肿瘤学界认可
戈利昔替尼单药肿瘤缓解率达42.9%,有望成为外周T细胞淋巴瘤的新疗法
DZD1516能够完全穿透血脑屏障,进军HER2阳性乳腺癌,神经系统转移
DZD2269可有效解除高浓度腺苷引起的免疫抑制,开启肿瘤免疫治疗的未来
公司宣布四个自主在研项目的重要研究发现和临床试验结果入选2022年度美国临床肿瘤学会(ASCO)大会,涉及的抗肿瘤候选药物包括舒沃替尼(DZD9008)、戈利昔替尼(DZD4205)、DZD1516和DZD2269,涵盖肺癌、血液瘤、乳腺癌等多个治疗领域,项目摘要已在ASCO官网公布。
ASCO年会是全球肿瘤领域最权威和最受期待的学术盛会之一,公司五个临床在研产品中有四个集中亮相2022 ASCO,其中舒沃替尼以口头报告首秀2021 ASCO后再次获选2022 ASCO壁报讨论(poster discussion),充分彰显了迪哲医药原研之光。
"今年公司多项在研成果荣登ASCO年会,再一次证明了迪哲在全球创新药领域的研发实力。基于转化科学和血脑屏障领域的国际领先优势,我们建立了具备全球竞争力的产品管线,其中两个产品处于全球关键性注册临床阶段,五个产品处于全球临床阶段。"公司创始人、董事长张小林博士表示,"多项临床研究结果也将推动癌症治疗的发展,为全球肿瘤患者带来新希望。"
一、2022 ASCO入选项目
(一)壁报讨论(Poster Discussion)
舒沃替尼是肺癌领域,且,获得中美双突破性疗法认定的国创新药,目前处于全球关键性注册临床阶段,近日研究成果在国际,期刊Cancer Discovery(《癌症发现》,IF:39.397)发表。本届ASCO年会发布舒沃替尼在既往含铂化疗失败后EGFR 20号外显子插入突变非小细胞肺癌人群的疗效分析结果,并且针对前线是否经过免疫治疗进行了亚组分析。临床数据显示,舒沃替尼100 mg及以上剂量组均可观察到抗肿瘤疗效,其中关键剂量300 mg组最佳肿瘤缓解率(ORR)达到48.4%,疾病控制率(DCR)达到90.3%。亚组分析显示,前线免疫治疗对舒沃替尼的有效性与安全性没有影响。
(二)壁报(Poster Session)
(1)戈利昔替尼
戈利昔替尼是T细胞淋巴瘤领域全球,且迄今为止,处于全球关键性注册临床阶段的高选择性JAK1抑制剂。本届ASCO年会发布戈利昔替尼治疗复发难治性外周T细胞淋巴瘤(r/r PTCL)的国际多中心I/II期临床研究数据。临床数据显示,截至2021年5月31日,戈利昔替尼肿瘤缓解率(ORR)达42.9%,最长DoR(缓解持续时间)超过14个月,在多种常见PTCL亚型中均观察到肿瘤缓解,并在既往接受过HDAC抑制剂、干细胞移植的患者中观察到不错的疗效信号。凭借其优异的有效性、安全性和耐受性,戈利昔替尼获美国食品药品监督管理局(FDA)快速通道认定,此前I/II期临床研究结果入选2021年第16届国际恶性淋巴瘤大会(ICML)与2022年第30届欧洲血液协会年会(EHA)口头报告。
(2)DZD1516
DZD1516是全球创新型具有完全穿透血脑屏障能力的高选择性HER2抑制剂。HER2 阳性乳腺癌发生,神经系统( CNS)转移的比例高达40%–60%,而现有大部分化疗或大分子靶向药物不能有效通过血脑屏障。公司基于特有的脑转移及脑膜转移模型技术平台设计并开发DZD1516,将在本届ASCO年会发布治疗HER2阳性转移性乳腺癌(MBC)的安全性和药代动力学(PK) 特征。国际多中心I期临床研究结果显示DZD1516在每日两次低于300毫克的给药剂量范围内表现出良好的耐受性,基于其对野生型EGFR有高于300倍以上的选择性,无患者发生腹泻或皮疹的不良反应事件。患者体内,DZD1516和其代谢物DZ2678的Kpuu,CSF(脑脊液与血浆中游离药物浓度的比值)分别约为2.13和0.66,表明DZD1516能够完全穿透血脑屏障。
(三)线上发布(online Publication)
DZD2269是全球创新型高选择性腺苷A2a受体(A2aR)拮抗剂,全球范围内尚无A2aR拮抗剂产品获批。细胞外腺苷是体内天然存在的免疫抑制物,虽然在正常组织或血液中浓度较低,但在肿瘤微环境 (TME) 中可能会高出 1,000 倍以上。本届ASCO年会发布的是在健康受试者中开展的I期、双盲、安慰剂对照研究,旨在评估DZD2269的安全性、PK以及对生物标志物的作用。初步研究结果表明,单剂量口服DZD2269(5 mg – 160 mg)安全性及耐受性良好,并且显示出良好的PD-PK相关性。单剂量80mg的DZD2269可实现持续24小时的90%的p-CREB抑制;36例健康受试者接受了单次口服剂量的DZD2269,未观测到3级及以上TEAE或严重不良事件(SAE)。上述临床数据支持DZD2269在肿瘤领域进一步临床开发。
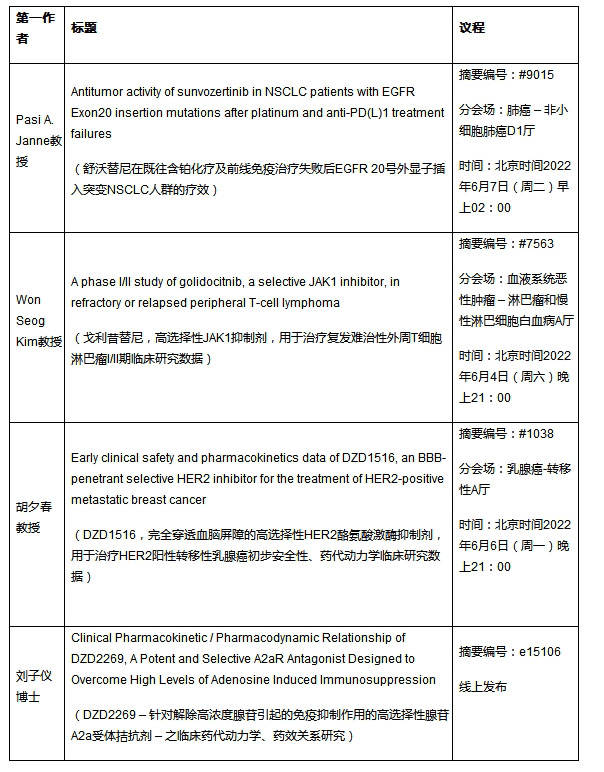
二、入选项目大会报告议程
关于迪哲医药
迪哲医药是一家处于临床开发阶段的全球创新型生物医药企业,专注于恶性肿瘤和免疫性疾病领域,致力于开发具备差异化竞争优势的全球创新药。基于行业领先的转化科学和新药分子设计与筛选技术平台,公司已建立了具备全球竞争力的在研管线,其中两大领先产品已处于全球关键性注册临床试验阶段。


















